这是 达医晓护 的第 5592 篇文章
肠道作为人体最大的消化器官,因其消化和发酵食物的功能特点,肠腔含有数目庞大的微生物群。在这个多元的微生态体系中,细菌是大众最为关注的对象。然而,科研人员发现,一群更微小的“隐形玩家”——肠道噬菌体(即感染细菌的病毒),正以独特的方式操控着肠道菌群的命运。噬菌体与细菌的互相作用,如同一场微观世界的“谍战”,深刻影响着人体的健康或疾病状态。 1. 噬菌体:细菌的精准“刺客” 噬菌体是地球上最古老的生物之一,其数量在肠道中可达细菌的10倍,每克粪便中含量高达十亿至百亿。微生物学家Colin Hill团队2019年对人类肠道微生物组测序比对到4万个病毒基因片段,其中仅有241个是之前已知的病毒。提示肠道噬菌体仍然是微生物界一片未知的深海。噬菌体结构和遗传物质简单,却拥有极高的宿主特异性,单个噬菌体株通常只攻击特定菌株或特定菌种。这种特性使其成为天然靶向的“细菌调节器”和肠道菌群动态平衡的维持者。当某种细菌过度繁殖时,以其为宿主的噬菌体会迅速增殖,通过“裂解”细菌(侵入后释放子代病毒,导致细菌破裂死亡)控制其数量,防止单一菌过度扩增垄断肠道资源。当疾病状态下,细菌的扩增超出自身调节范围后,则有赖于外在干预手段。 肠道噬菌体还能够作为基因水平转移的媒介。部分温和噬菌体(溶原性噬菌体)会将自身DNA整合到细菌基因组中,悄无声息地潜伏。这些基因可能赋予细菌新的功能(如抗生素耐药性、毒素产生能力),甚至改变细菌的致病性。 2. 噬菌体与细菌的“攻防战”:无声的军备竞赛 面对噬菌体的精准打击,细菌并非被动挨打,而是演化出多种防御机制: (1)吸附抑制 吸附是噬菌体感染细菌的第一步,细菌通过下调或修饰细胞壁上被噬菌体识别的受体,或者分泌特定物质阻止噬菌体与细菌接触,能够抵御噬菌体对细菌的吸附。 (2)CRISPR-Cas系统 细菌利用这段“分子记忆”记录曾感染过的噬菌体基因片段,下次遭遇时可直接剪切其DNA,堪称细菌的“免疫系统”。 (3)限制性内切酶 可识别并切割噬菌体的特定DNA序列。 (4)流产感染 抑制噬菌体复制周期的各个环节,往往同时导致宿主细胞的死亡,从而使其余未受感染的细菌逃脱噬菌体感染。 面对细菌的对抗策略,噬菌体并没有坐以待毙,而是通过快速突变受体结合蛋白,逃逸细菌防御系统的识别,多方面对抗吸附抑制、CRISPR-Cas系统和流产感染系统。这种军备竞赛推动了两者的协同进化。 3. 噬菌体-细菌互作:健康与疾病的“双刃剑” (1)维护肠道稳态 噬菌体通过调控细菌组成,间接影响宿主的代谢(如短链脂肪酸合成)、免疫发育(如调节T细胞活性)。例如,肥胖人群的肠道噬菌体群落与瘦人显著不同,提示其可能通过靶向裂解特定细菌参与代谢调控。 (2)疾病中的潜在角色 近年来,肠道噬菌体在炎症性肠病(IBD)、慢性肝病、糖尿病等疾病中的功能被广泛报道。以IBD为例,患者肠道中噬菌体组结构紊乱,丰度和多样性降低。将健康人的噬菌体移植给IBD患者后,引发乳杆菌属(Lactobacillus)前噬菌体的显著增加,伴随乳杆菌科(Lactobacillaceae)和毛螺菌科(Lachnospiraceae)丰度增高,菌群结构更接近健康状态。在感染性疾病中,噬菌体携带的毒力基因(如志贺毒素基因)可能通过侵染大肠杆菌等病原体,加重感染症状。 (3)治疗新思路 针对耐药菌感染,科学家尝试用噬菌体精准清除病原菌(如肺炎克雷伯菌)的噬菌体疗法。相比抗生素,其优势在于不破坏共生菌群。目前已有临床试验探索其在克罗恩病、腹泻等疾病中的应用。 4. 未来展望 尽管肠道噬菌体的研究仍有较大空间,但已展现出巨大潜力。然而,超过99%的肠道噬菌体尚未被培养,功能难以解析;个体间肠道噬菌体差异大,需开发个性化调控策略。 随着宏基因组学和培养技术的进步,肠道噬菌体这片“隐秘的宇宙”终将揭开神秘面纱。或许在不远的未来,我们能够通过定制噬菌体鸡尾酒,重塑肠道生态,实现多种疾病的精准干预。 您认为噬菌体会成为下一代“智能抗生素”吗?欢迎读者留言讨论。 噬菌体吸附到细菌细胞壁的透射电镜图。(图片来源:https://commons.wikimedia.org/wiki/File:Phage.jpg) 作者:上海市第十人民医院 陈倩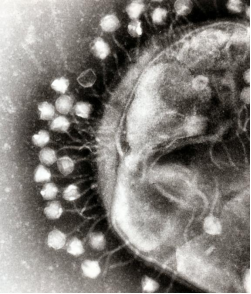
部分图片摘自网络,如有侵权请告知,予以删除。
所有人名和地名均为化名,如有雷同,纯属巧合。
肠内乾坤杂志主编:陈启仪
发表评论





 收藏
收藏
 赞
赞